⑷ 洗脱、收集、鉴定
洗脱条件的选择,也是影响层析效果的重要因素。当我们选定好洗脱液后,洗脱的方式可分为简单洗脱、分步洗脱和梯度洗脱三种。
简单洗脱:柱子始终用同样的一种溶剂洗脱,直到层析分离过程结束为止。如果被分离物质对固定相的亲合力差异不大,其区带的洗脱时间间隔(或洗脱体积间隔)也不长,采用这种方法是适宜的。但选择的溶剂必须很合适方能使各组分的分配系数较大。否则应采用下面的方法。
分步洗脱:这种方法按照递增洗脱能力顺序排列的几种洗脱液,进行逐级洗脱。它主要对混合物组成简单、各组分性质差异较大或需快速分离时适用。每次用一种洗脱液将其中一种组分快速洗脱下来。
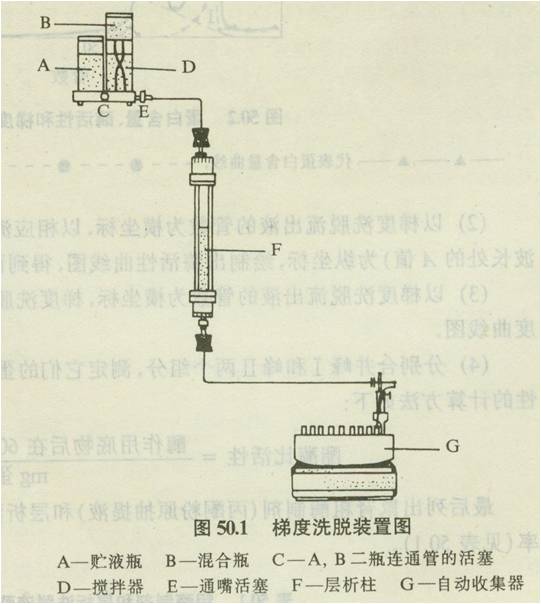
梯度洗脱:当混合物中组分复杂且性质差异较小时,一般采用梯度洗脱。它的洗脱能力是逐步连续增加的,梯度可以指浓度、极性、离子强度或pH值等。最常用的是浓度梯度。在水溶液中,亦即离子强度梯度。
当对所分离的混合物的性质了解较少时,一般先采用线性梯度洗脱的方式去尝试,但梯度的斜率要小一些,尽管洗脱时间较长,但对性质相近的组分分离更为有利。
同时还应注意洗脱时的速率。前面我们已经谈到,流速的快慢将影响理论塔板高度,从而影响分辨率。事实上,速度太快,各组分在固液两相中平衡时间短,相互分不开,仍以混合组分流出。速度太慢,将增大物质的扩散,同样达不到理想的分离效果。只有多次试验才会得到合适的流速。总之,我们必须经过反复的试验与调整(可以用正交试验或优选法),才能得到最佳的洗脱条件。还应强调的一点是,在整个洗脱过程中,千万不能干柱,否则分离纯化将会前功尽弃。
在生化实验中,基本上我们都是采用部分收集器来收集分离纯化的样品。由于检测系统的分辨率有限,洗脱峰不一定能代表一个纯净的组分。因此,每管的收集量不能太多,一般1ml-5ml / 管。如果分离的物质性质很相近,可低至0.5ml / 管。这视具体情况而定。在合并一个峰的各管溶液之前,还要进行鉴定。例如,一个蛋白峰的各管溶液,我们要先用电泳法对各管进行鉴定。对于是单条带的,认为已达电泳纯,合并在一起。其他的另行处理。对于不同种类的物质采用相应的鉴定方法,在这里不再叙述。最后,为了保持所得产品的稳定性与生物活性,我们一般采用透析除盐、超滤或减压薄膜浓缩,再冰冻干燥,得到干粉,在低温下保存备用。
用pH7.8,2.5mmol/L(100mL)一200mmol/L(100mL)的磷酸钠缓冲液进行梯度洗脱。流速1mL/min,每管收集3mL。测定洗脱液的蛋白质含量和酶活,并绘制曲线(用紫外分光光度计测各管的 OD 280 , OD 280 数值高的管进行酶活测定 )。
⑹ 基质(吸附剂、交换树脂或凝胶等)的再生
许多基质(吸附剂、交换树脂或凝胶等)可以反复使用多次,而且价格昂贵,所以层析后要回收处理,以备再用,严禁乱倒乱扔。这也是一个科研工作者的科学作风问题。
2、植物组织SOD活性测定:超氧化物歧化酶活性测定的方法有多种,其中以化学法应用O·最为普遍。化学测定法包括两个方面:一方面是产生超氧自由基,
如黄嘌呤氧化酶起作用时会产生O,肾上腺素自氧化和邻苯三酚在碱性条件下自
氧化都会产生O .;另一方面是对O·的检测,多数是利用反应液中能与O·起作用,并易于被检测的指示物质的浓度变化来测定SOD活性。常用的方法有:黄嘌呤-黄嘌呤氧化酶-细胞色素C法,邻苯三酚自氧化法,超氧化钾直接滴定法,氯化硝基氮蓝四唑-核黄素法。
可采用氮蓝四唑(NBT)光还原法。在该反应系统中,核黄素照光产生02-,NBT在光照下被02-还原为蓝甲月替,产物在560nm下有吸收峰。通过测定加入酶液后蓝甲月替含量的变化,可计算出SOD的活性。
3、分析方法
蛋白质含量测定:采用紫外线吸收法。
酶纯度用比活力表示。比活力=酶活/蛋白质含量。
三、设备
高速组织捣拌机、电热鼓风干燥箱、LD4-40离心机、酸度计、恒温水浴锅、天平、冷冻离心机、可见分光光度计、微量进样器、自动部分收集器、TH-梯度混合器、HL-IS恒流泵、紫外可见分光光度计、层析柱、光照箱

四、材料、试剂
1、圆葱
2、硫酸钠(1%)、硝酸钠(1%)、三氯乙酸(0.5%)、乙醇(5%)、乙醚(5%)、、无水碳酸钠、NaOH、CuSO4、酒石酸钠钾、钨酸钠(Na2WO4·2H2O)、钼酸钠(Na2MoO4·2H2O)磷酸溶液、浓盐酸。硫酸锂、液体溴、NaOH标准溶液、酚酞、标准牛血清蛋白、Na2HPO4.12H2O、NaH2PO4.2H2O氯化硝基氮蓝四唑、乙二胺四乙酸二钠、 核黄素、dl-甲硫氨酸、丙酮(0.5%)0.5mmol/L NaCl、1mol/L HCl溶液、1mol/L NaOH溶液
3、溶剂配制
⑴50mmol/L PBS溶液(pH=7.8): ①取17.9070gNa2HPO4.12H2O定容至1000ml; ②取1.9501gNaH2PO4.2H2O定容至250ml.用②滴定①pH至=7.8,即为50mmol/L磷酸缓冲溶液.
⑵2.25mmol/L NBT溶液:取0.1840g氯化硝基氮蓝四唑用pH为7.8的50mmol/L PBS溶液定容至100ml.
⑶ 0.003mmol/L EDTA:取0.0011g乙二胺四乙酸二钠用pH为7.8的50mmol/L PBS溶液定容至1000ml.
⑷60mmol/L 核黄素:取0.0023g核黄素用pH为7.8的50mmol/L PBS溶液定容至100ml.
⑸14.5mmol/L dl-甲硫氨酸:取0.2163gdl-甲硫氨酸用水定容至100ml.
⑹1mg/ml标准牛血清蛋白:准确称取0.05g牛血清蛋白定容至50ml。
⑺pH7.8,2.0mmol/L的磷酸钠缓冲液:
A液:2.0mmol/L磷酸钠(NaH2PO4.H2O 0.287g定容至1000ml)
B液:2.0mmol/L磷酸氢二钠(Na2HPO4.12H2O 0.711g定容至1000ml)
按表1方法配制不同pH值缓冲溶液,取A液x ml和B液y ml,稀释成200ml溶液备用。
表1 不同pH值缓冲溶液配制
|
pH
|
X ml
|
Y ml
|
|
7.8
|
8.5
|
91.5
|
⑻pH7.8,200mmol/L的磷酸钠缓冲液:
A液:0.2mol/L磷酸钠(NaH2PO4.H2O 28.70g定容至1000ml)
B液:0.2mol/L磷酸氢二钠(Na2HPO4.12H2O 71.1g定容至1000ml)
按表1方法配制不同pH值缓冲溶液,取A液xml和B液yml,稀释成200ml溶液备用。
表2不同pH值缓冲溶液配制
|
pH
|
X ml
|
Yml
|
|
7.8
|
8.5
|
91.5
|
